যে শক্তি কোনো যান্ত্রিক পদ্ধতি ছাড়াই এক বস্তু থেকে অন্য বস্তুতে সঞ্চালিত হয় ,যা গ্রহণ করলে বস্তু উত্তপ্ত হয় এবং বর্জন করলে ঠান্ডা হয় তাকে তাপ বলে ।
সাধারণত তাপ তিন প্রকারের হয়-
1. বোধগম্য তাপ (Sensible heat) : যে তাপ প্রয়োগে বস্তুর তাপমাত্রা বেড়ে যায় সেই তাপকে বোধগম্য তাপ বলে । ক্যালরিমিটারের সাহায্যে এই তাপ পরিমাপ করা যায় ।
2.লীনতাপ (Latent Heat): যে তাপ প্রয়োগে উষ্নতার পরিবর্তন না ঘটিয়ে অবস্থার পরিবর্তন ঘটায় সেই তাপকে লীন তাপ বলে ।ক্যালরিমিটার দিয়ে এই তাপ পরিমাপ করা যায় না ।

3.বিকীর্ণ তাপ (Radiant Heat):উৎস থেকে যে তাপ বিকিরণ পদ্ধতিতে সঞ্চালিত হয় তাকে বিকীর্ণ তাপ বলে । যেমন সূর্য্য থেকে পৃথিবীতে আগত তাপ ।ক্যালরিমিটারের সাহায্যে এই তাপ পরিমাপ করা যায় না ।
তাপের একক : CGS পদ্ধতিতে তাপের একক ক্যালোরি । SI পদ্ধতিতে তাপের একক জুল ।
ক্যালোরি - 1 গ্রাম বিশুদ্ধ জলের উষ্নতা 1⁰C ( 14.5⁰C থেকে 15.5⁰C) বৃদ্ধি করতে যে তাপের প্রয়োজন হয় তাকে এক ক্যালোরি বলে ।
জুল - 1 কিগ্ৰা বিশুদ্ধ উষ্নতা 1 K বা 1⁰C বৃদ্ধি করতে যে পরিমান তাপের প্রয়োজন হয় তার 1/4200 অংশকে এক জুল বলে । 1 ক্যালোরি = 4.2 জুল বা 1 জুল = 0.24 ক্যালোরি ।
তাপের ফল (Effect of Heat):
1. উষ্নতার পরিবর্তণ : অবস্থার পরিবর্তণ না হলে তাপ প্রয়োগের ফলে বস্তুর উষ্নতা বাড়ে ও তাপ অপসারিত করলে উষ্নতা কমে ।
2 অবস্থার পরিবর্তণ : তাপ প্রয়োগে অবস্থার পরিবর্তণ হয় , কঠিন পদার্থ তরলে এবং তরল পদার্থ গ্যাসীয় অবস্থায় পরিণত হয় ।
3.আয়তনের পরিবর্তণ : সাধারণত তাপ দিলে বস্তুর আয়তন বাড়ে এবং তাপ বের করে নিলে বস্তুর আয়তন কমে ।
ব্যতিক্রম - ঢালাই লোহা , বরফ ,পিতল ,বিসমাথ প্রভৃতি পদার্থের উপর তাপ প্রয়োগ করলে আয়তন কমে ।
4. রাসায়নিক পরিবর্তণ : অনেকক্ষেত্রে তাপ দিলে রাসায়নিক পরিবর্তণ সাধিত হয় । যেমন - ZnCO₃ + তাপ ⟶ ZnO + CO₂ ,HgO +তাপ ⟶ Hg + O₂

5.দহন : দাহ্য পদার্থে তাপ প্রয়োগ করলে জ্বলে যায় ।
6.বৈদ্যুতিক ধর্মের পরিবর্তণ : তাপ প্রয়োগে পরিবাহী পদার্থের রোধ বৃদ্ধি পায় ।
7.চৌম্বক ধর্মের পরিবর্তণ : চুম্বকের উপর তাপ প্রয়োগ করলে একটি নিৰ্দিষ্ট উষ্নতায় ওর চৌম্বক ধৰ্ম লোপ পায় ।
8.আলোকশক্তির সৃষ্টি : বৈদ্যুতিক বাতিতে ফিলামেন্ট অত্যাধিক উত্তপ্ত হলে আলো বিকিরিত হয় ।
গৃহীত ও বর্জিত তাপ :
তাপ প্রয়াগে কোনো বস্তুর যদি অবস্থার পরিবর্তণ না হয় তাহলে গৃহীত ও বর্জিত তাপ নিম্নলিখিত বিষয়গুলির ওপর নির্ভর করে ।
1. ভরের উপর নির্ভরশীলতা :তাপমাত্রা বৃদ্ধি বা হ্রাস অপরিবর্তিত থাকলে এবং একই উপাদানের বস্তুর দ্বারা গৃহীত বা বর্জিত তাপ বস্তুটির ভরের সমানুপাতিক হয় । অর্থাৎ H ∝ m (উষ্নতা বৃদ্ধি t, বস্তুর উপাদান = স্থির ), H = গৃহীত বা বর্জিত তাপ , m = বস্তুর ভর ।
2.উষ্নতার উপর নির্ভরশীলতা :.বস্তুর ভর অপরিবর্তিত থাকলে ও একই উপাদান দ্বারা গঠিত বস্তুর দ্বারা গৃহীত ও বর্জিত তাপ বস্তুটির তাপমাত্রা বৃদ্ধি বা হ্রাসের সঙ্গে সমানুপাতিক । অর্থাৎ H ∝ t ( m , বস্তুর উপাদান = স্থির )
3.উপাদানের উপর নির্ভরশীলতা(আপেক্ষিক তাপ ) - বস্তুর ভর ও তাপমাত্রা বৃদ্ধি সমান থাকলে বস্তু কর্তৃক গৃহীত ও বর্জিত তাপ বস্তুটির উপাদানের উপর নির্ভর করে ।
উপরের 1 নং ও 2 নং অনুচ্ছেদ থেকে পাই ,
H ∝ mt
বা H = s mt ( s একটি ধ্রুবক যা বস্তুটির উপাদানের উপর নির্ভরশীল )
বা s = H/(mt)
m = 1 এবং t = 1 হলে s = H
অর্থাৎ একক ভরের কোনো বস্তুর একক উষ্নতা বৃদ্ধি করতে যে পরিমান তাপের প্রয়োজন হয় তাকে বস্তুটির আপেক্ষিক তাপ বলে । আপেক্ষিক তাপ উপাদানের উপর নির্ভর করে । বিভিন্ন ধাতুর আপেক্ষিক তাপ বিভিন্ন হয় ।
অতএব গৃহীত ও বর্জিত তাপের সমীকরণটি হল -
H= mst ( m = বস্তুর ভর ,s = বস্তুর আপেক্ষিক তাপ, t = তাপমাত্রা বৃদ্ধি বা হ্রাস )
আপেক্ষিক তাপের একক - ক্যালোরি / গ্রাম ⁰C ( cal /g⁰C) [CGS পদ্ধতি ],
জুল/কেজি কেলভিন ( J/kgK) [ SI পদ্ধতি ]
ক্যালরিমিতির মূল নীতি :
দুটি ভিন্ন উষ্নতার বস্তুকে পরস্পর সংস্পর্শে আনলে উহাদের মধ্যে তাপের আদান প্রদান ঘটে । বেশি উস্নতার বস্তুটি তাপ বর্জন করে এবং কম উষ্নতার বস্তুটি তাপ গ্রহণ করে । এই গ্রহণ বর্জন চলতে থাকে যতক্ষন না উভয় বস্তুর উষ্নতা সমান হয় । এমতাবস্থায় উষ্ন বস্তু কর্তৃক বর্জিত তাপ = শীতল বস্তু কর্তৃক গৃহীত তাপ । এটিই হল ক্যালরিমিতির মূল নীতি ।
গাণিতিক সমীকরণ :
ধরি উষ্ন বস্তুটির ভর = m₁ , উপাদানের আপেক্ষিক তাপ = S₁ ,উষ্নতা = t₁
শীতল বস্তুটির ভর = m₂ , আপেক্ষিক তাপ = S₂ এবং উষ্নতা = t₂ (t₁ > t₂)
তাপ গ্রহণ বর্জনের পরে তাপীয় সাম্যাবস্থায় উভয় বস্তুর উষ্নতা = t ( t₁> t >t₂)
উষ্নবস্তু বস্তু কর্তৃক বর্জিত তাপ = m₁S₁(t₁ - t ),
শীতল বস্তু কর্তৃক গৃহীত তাপ = m₂S₂( t - t₂),
ক্যালরিমিতির মূলনীতি থেকে পাই ,
বর্জিত তাপ = গৃহীত তাপ
অর্থাৎ m₁S₁(t₁ - t ) = m₂S₂( t - t₂)

ছবিতে আপেক্ষিক তাপ c₁ ও c₂ দ্বারা বোঝানো হয়েছে ।
কার্য ও তাপের মধ্যে সম্পর্ক :
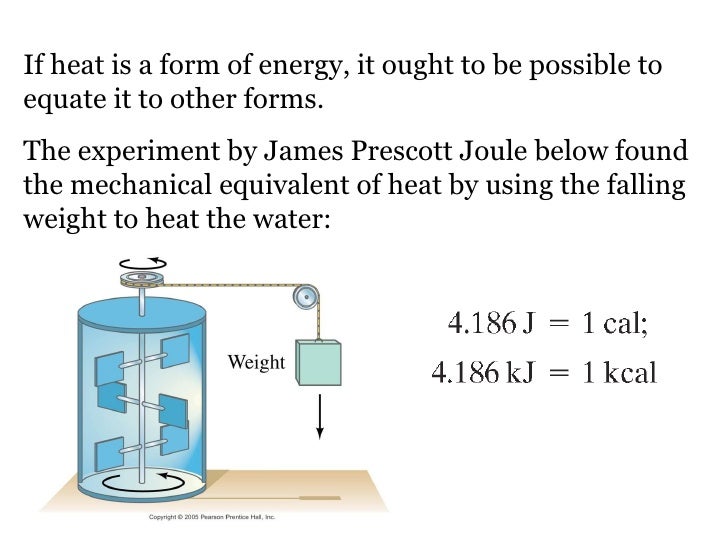
উপর থেকে যখন কোনো বস্তু মাটিতে পড়ে তখন যান্ত্রিক শক্তি তাপশক্তি , শব্দ শক্তি , আলোকশক্তি ইত্যাদিতে রূপান্তরিত হয় । যান্ত্রিক শক্তি অর্থাৎ কার্য ও তাপ পরস্পর রূপান্তর যোগ্য । এই রূপান্তর জুল সু্ত্র দ্বারা নির্ধারিত হয় ।
জুলের সূত্র : কার্য সম্পূর্ণরূপে তাপে বা তাপ সম্পূর্ণরূপে কার্যে রূপান্তরিত হলে ,কৃত কার্য ও উৎপন্ন তাপ পরস্পর সমানুপাতিক হয় ।
যদি W পরিমাণ কার্য সম্পূর্ণ রূপান্তরিত হয়ে H পরিমাণ তাপ উৎপন্ন করে তাহলে ,
W ∝ H
বা ,W = JH ( J একটি ধ্রুবক )
বা , J = W/H
এই J কে বলা হয় তাপের যান্ত্রিক তুল্যাঙ্ক । H = 1 হলে J = W , অর্থাৎ একক পরিমাণ তাপ উৎপাদন করতে যে পরিমাণ কার্য সম্পাদন করতে হয় তাকে তাপের যান্ত্রিক তুল্যাঙ্ক বলে ।
J এর মান তাপ ও কার্যের এককের উপর নির্ভর করে । SI পদ্ধতিতে তাপ ও কার্য উভয়ের একক জুল । সুতরাং SI পদ্ধতিতে J = 1 ,অর্থাৎ এক জুল কার্য সম্পুর্ণ রূপে তাপে রূপান্তরিত হলে এক জুল তাপশক্তি উৎপন্ন করে ।
CGS পদ্ধতিতে তাপের একক ক্যালোরি এবং কার্যের একক আর্গ বা জুল , এক্ষেত্রে J = 4.186 x 10⁷ আর্গ /ক্যালোরি বা 4.186 জুল /ক্যালোরি
অর্থাৎ J = 4.2 J/cal.
লীন তাপ (Latent Heat):
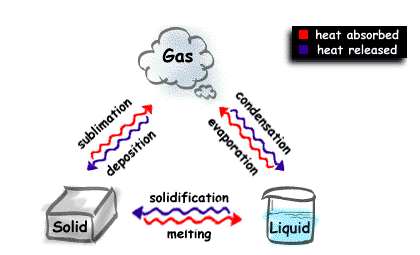
পদার্থের অবস্থার পরিবর্তণ - তাপ প্রয়োগ বা নিষ্কাশনের ফলে পদার্থের এক অবস্থা থেকে অন্য অবস্থায় রূপান্তর হওয়ার ঘটনাকে অবস্থার পরিবর্তণ বলে ।
তাপ প্রয়োগে পদার্থের উচ্চ অবস্থান্তর ঘটে । যেমন - কঠিন থেকে তরলে রূপান্তর , বা তরল থেকে বাস্পে রূপান্তর ।
তাপ নিষ্কাশন করলে নিম্ন অবস্থান্তর ঘটে । যেমন - তরল অবস্থা থেকে কঠিন অবস্থায় রূপান্তর ।
অবস্থার পরিবর্তণের বৈশিষ্ট :
1. অবস্থার পরিবর্তণের সময় তাপ গৃহীত বা বর্জিত হয়।
2.অবস্থার পরিবর্তনের সময় উষ্নতার কোনো পরিবর্তণ হয় না ।
3.অবস্থার পরিবর্তনের সময় আয়তনের হ্রাস বা বৃদ্ধি হয় ।
অবস্থার পরিবর্তনের সময়ে পদার্থ তাপ গ্রহণ বা বর্জন করা সত্বেও পদার্থের উষ্নতার কোনো পরিবর্তণ হয় না কারণ এই তাপ পদার্থের অণুগুলির নিৰ্দিষ্ট জ্যামেতিক সজ্জা ভেঙ্গে পদার্থের অবস্থান্তর ঘটায় ।
লীনতাপ(Latent Heat) : প্রমাণ চাপে কোনো পদার্থের একক ভরের উষ্নতার পরিবর্তণ না ঘটিয়ে শুধুমাত্র অবস্থার পরিবর্তণ ঘটাতে যে পরিমান তাপ প্রয়োগ বা নিষ্কাশন করতে হয় তাকে ওই পদার্থের লীনতাপ বলে ।

CGS পদ্ধতিতে লীনতাপের একক ক্যালোরি-গ্রাম⁻¹ ( Cal g⁻¹)
SI পদ্ধতিতে একক জুল- কিলোগ্রাম⁻¹(J kg⁻¹)
লীনতাপের মাত্রা = শক্তির মাত্রা / ভরের মাত্রা = [ML²T⁻²]/[M] = [L²T⁻²]
লীনতাপের প্রকারভেদ :
পদার্থের অবস্থান্তর অনুসারে লীনতাপ চার প্রকারের হয় । 1.গলনের লীনতাপ 2. কঠিনীভবনের লিনতাপ 3. বাষ্পীভবনের লীনতাপ 4. ঘনীভবনের লীনতাপ
1.গলনের লীনতাপ - প্রমাণ চাপে একক ভরের কোনো কঠিন পদার্থকে স্থির উস্নতায় সম্পূর্ণভাবে তরলে পরিণত করতে যে পরিমাণ তাপ প্রয়োগ করতে হয় তাকে ওই কঠিনের গলনের লীনতাপ বলে । বরফ গলনের লীনতাপ 80 ক্যালোরি /গ্রাম (CGS পদ্ধতি ) । SI পদ্ধতিতে বরফ গলনের লীনতাপ 3.36 x 10⁵ জুল /কিলোগ্রাম ।
2.কঠিনীভবনের লীনতাপ : প্রমাণ চাপে কোনো একক ভরের তরল পদার্থকে তার হিমাঙ্কে স্থির রেখে সম্পূর্ণভাবে কঠিনে পরিণত করতে যে পরিমাণ তাপ নিষ্কাশন করতে হয় সেই পরিমাণ তাপকে ওই তরলের কঠিনীভবনের লীন তাপ বলে ।CGS পদ্ধতিতে জলের কঠিনীভবনের লীন তাপ 80 ক্যালোরি /গ্রাম |
বাস্পীভবনের লীনতাপ : স্থির তাপমাত্রায় এবং প্রমাণ চাপে একক ভরের কোনো তরল পদার্থকে সম্পূর্ণভাবে বাস্পে পরিণত করতে যে তাপ প্রয়োগ করতে হয় সেই পরিমান তাপকে ওই তরলের বাষ্পীভবনের লীনতাপ বলে । জলের বাষ্পীভবনের লিনতাপ 537 ক্যালোরি /গ্রাম (CGS পদ্ধতি )
ঘনীভবনের লীনতাপ :প্রমাণ চাপে একক ভরের কোনো বাস্পকে উষ্নতার পরিবর্তণ না ঘটিয়ে সম্পূর্ণভাবে তরল অবস্থায় পরিণত করতে যে পরিমাণ তাপ নিষ্কাশন করতে হয় তাকে ওই বাষ্পের ঘনীভবনের লীনতাপ বলে । CGS পদ্ধতিতে জলীয় বাষ্পের ঘনীভবনের লীনতাপ 537 ক্যালোরি/গ্রাম ।
লীনতাপ ও বোধগম্য তাপের মধ্যে পার্থক্য :
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
সম্পৃক্ত বাস্প ও অসম্পৃক্ত বাস্প (Saturated Vapour and unsaturated Vapour):
সম্পৃক্ত বাষ্প - নিৰ্দিষ্ট উস্নতায় কোনো নিৰ্দিষ্ট আবদ্ধ আয়তনের মধ্যে সর্বোচ্চ পরিমাণ জলীয় বাষ্প উপস্থিত থাকলে ওই জলীয় বাষ্পকে সম্পৃক্ত বাস্প বলে ।ওই বাস্প ওই স্থানে যে চাপ দেয় তাকে সম্পৃক্ত বাস্প চাপ বলে ।
অসম্পৃক্ত বাষ্প - কোনো আবদ্ধ স্থানে একটি নিৰ্দিষ্ট উষ্নতায় সর্বোচ্চ যে পরিমাণ জলীয় বাস্প থাকতে পারে তার থেকে কম জলীয় বাষ্প থাকলে ওই বাষ্পকে অসম্পৃক্ত বাস্প বলে । অসম্পৃক্ত বাষ্প যে চাপ দেয় তাকে অসম্পৃক্ত বাষ্প চাপ বলে ।
আর্দ্রতা - আর্দ্রতা দ্বারা কোনো সময়ে কোনো স্থানের বায়ুতে অবস্থিত জলীয় বাষ্পের পরিমাণ বোঝায় ।
আপেক্ষিক আর্দ্রতা (Relative Humidity):
কোনো নিৰ্দিষ্ট উষ্নতায় কোনো নিৰ্দিষ্ট আয়তনের বায়ুতে উপস্থিত জলীয় বাষ্পের পরিমাণ এবং ওই একই উষ্নতায় ওই আয়তনের বায়ুকে সম্পৃক্ত করতে প্রয়োজনীয় জলীয় বাষ্পের ভর এই দুইয়ের অনুপাতকে আপেক্ষিক আর্দ্রতা বলে ।
আপেক্ষিক আর্দ্রতা = নিৰ্দিষ্ট উস্নতায় নিৰ্দিষ্ট আয়তনের বায়ুতে উপস্থিত জলীয় বাষ্পের ভর / ওই উষ্নতায় ওই আয়তনের বায়ুকে সম্পৃক্ত করতে প্রয়োজনীয় জলীয় বাষ্পের ভর
আপেক্ষিক আর্দ্রতা শতকরা হিসাবে প্রকাশ করা হয় ,তাই উপরের ভগ্নাংশকে 100 দ্বারা গুন্ করা হয় ।যেমন - বায়ুর আপেক্ষিক আর্দ্রতা 20⁰c উষ্নতায় 80 % এর অর্থ হল বায়ুকে 20⁰c উষ্নতায় সম্পৃক্ত করতে যে জলীয় বাষ্পের প্রয়োজন তার 80 % উপস্থিত আছে ।

শিশিরাঙ্ক(Dew Point):
যে উষ্নতায় কোনো নিৰ্দিষ্ট পরিমাণ বায়ুতে উপস্থিত জলীয় বাষ্প দ্বারা সম্পৃক্ত হয় সেই উষ্নতাকে শিশিরাঙ্ক বলে ।
শিশির (Dew):
কোনো স্থানের বায়ুর উষ্নতা শিশিরাঙ্কের নিচে নামলে ওই বায়ুর মধ্যে অবস্থিত অতিরিক্ত জলীয় বাষ্প ঘনীভূত হয়ে জলের বিন্দু রূপে ভূপৃষ্ট সংলগ্ন বস্তু বা ঘাসের উপর জমে জয় , এই জল বিন্দুগুলিকে শিশির বলে ।
দিনের বেলায় পৃথিবীর তাপমাত্রা অনেক বেশি হয় ।সূর্য অস্ত যাওয়ার পরে পৃথিবী তাপ বিকিরণ করে ক্রমশ শীতল হয় । অর্থাৎ বাতাস ক্রমশ সম্পৃক্ত অবস্থার দিকে অগ্রসর হয় , যখন পরিবেশের উষ্নতা শিশিরাঙ্কের নিচে নেমে যায় বায়ুর অতিরিক্ত জলীয় বাস্প জলের বিন্দুতে পরিণত হয়ে ঘাস ও গাছের পাতায় জমা হয় ।একে শিশির বলে ।
শিশির জমার শর্ত :
1. স্থির বাতাস - বাতাস স্থির থাকলে বাতাসের উষ্নতা শিশিরাঙ্কের নিচে চলে যাবার সম্ভাবনা বেশি হয় । তাই স্থির বাতাস শিশির পড়ার সহায়ক ।2.বায়ুতে জলীয় বাষ্পের পরিমাণ : - বাতাসে বেশি পরিমাণ জলীয় বাস্প থাকলে অল্প উষ্নতা কমলেই বায়ুর উষ্নতা শিশিরাঙ্কের নিচে নামে ফলে শিশির পড়ার সহায়ক হয় ।
3.তাপের উত্তম বিকিরক ও কুপরিবাহী বস্তুর উপস্তিতি - বস্তু উত্তম বিকিরক হলে তাড়াতাড়ি ঠান্ডা হয় এবং বস্তু কুপরিবাহী হলে বস্তু সহজে তাপ গ্রহণ করে না , ফলে শিশির পড়ার সহায়ক হয় ।
কুয়াশা(fog) -
বায়ুমণ্ডলের বিস্তীর্ণ অঞ্চলের উষ্নতা কোনো কারণে শিশিরাঙ্কের নিচে গেলে বায়ুর অতিরিক্ত জলীয় বাস্প ঘনীভূত হয়ে বিন্দু বিন্দু জল কণায় পরিণত হয় । ওই জল কণাগুলি বাতাসে ভাসমান ধূলিকণা , কয়লার গুঁড়ো ইত্যাদির সঙ্গে লেগে গিয়ে বাতাসে ভাসতে থাকে ,একেই কুয়াশা বলে । সূর্য ওঠার পর বায়ুমণ্ডলের উষ্নতা শিশিরাঙ্কের বেশি হলে কুয়াশা থাকে না , কারণ উষ্নতা বেশি হলে জল কণাগুলি বাষ্পীভূত হয়ে যায় ।
ধুঁয়াশা (Smog):
শহরাঞ্চলে এবং শিল্পাঞ্চলের বাতাসে প্রচুর পরিমাণে সূক্ষ্ম ধূলিকণা ,কয়লার গুঁড়ো ও তড়িতাহিত কণা ভাসতে থাকে ।এই গুলির উপর জলীয় বাষ্প জমার ফলে ঘন কুয়াশা সৃষ্টি হয় ,একে ধুঁয়াশা বলে ।
জলের ব্যতিক্রান্ত প্রসারণ(Anomalous Expansion of water) :
কোনো তরলে তাপ প্রয়োগ করলে ওই তরল আয়তনে প্রসারিত হয় , তাপ হ্রাস করলে আয়তনে সংকুচিত হয় । এটাই সাধারণ নিয়ম । জলের ক্ষেত্রে একটি নিৰ্দিষ্ট উষ্নতার পাল্লায় এই সাধারণ নিয়মের ব্যতিক্রম দেখা যায় । 0⁰C থেকে 4⁰C এর মধ্যে উষ্নতা বৃদ্ধি করলে জলের আয়তন না বৃদ্ধি পেয়ে কমে যায় , 4⁰C এ আয়তন সর্বনিম্ন হয় । অর্থাৎ 4⁰C এ জলের ঘনত্ব সর্বচ্চো হয় । জলের এই প্রাসারণকে ব্যতিক্রান্ত বলে ।

জলজ প্রাণীর উপর জলের ব্যতিক্রান্ত প্রসারণের ফল :

শীতপ্রধান দেশে অনেক সময় পরিবেশের উষ্নতা হিমাঙ্কের নিচে নেমে যায় ।ফলে জলাশয়ের জল বরফ হয়ে যায় । পরিবেশের উষ্নতা কমতে কমতে যখন 4⁰C হয় জল সবচেয়ে ভারী হয়ে যায় , ভারী জল পুকুরের তলদেশে চলে যায় ,নিচের হালকা জল উপরে উঠে আসে । উপরে উঠে আসা জলও 4⁰C উষ্নতা লাভ করে নিচে গমন করে।এই ভাবে সমস্ত জল 4⁰C উষ্নতা লাভ করে । উপরের অংশের জলের উষ্নতা আরো কমে যায় তখন জল ভারী না হয়ে হালকা হয় ,ফলে উপরের জল আর নিচে যেতে পারে না ।এই ভাবে উপরের জলের উষ্নতা 0⁰C হলে তা বরফে পরিণত হয় ।বরফ হালকা বলে জলের উপর ভাসে ।অর্থাৎ পুকুরের উপরের অংশের জল বরফ হয় ,নিচের জল বরফ হয় না কারণ বরফ তাপের কুপরিবাহী বলে তলদেশের তাপ বায়ুমণ্ডলে আসতে পারে না ।নিচের জলের উষ্নতা ক্রমশ বেড়ে একেবারে তলদেশের উষ্নতা 4⁰C হয় ।ফলে তলদেশের জলে মাছ ইত্যাদি জলজ প্রাণীদের বেঁচে থাকতে কোনো অসুবিধা হয় না ।
অনুশীলনী
সঠিক উত্তরটি নির্বাচন কর(MCQ) : https://forms.gle/XtSn3KScDbs2QQ8y7
1. আপেক্ষিক তাপের CGS একক হল -
A) ক্যালোরি/গ্রাম ⁰C B) জুল/কেজি K C) জুল / ⁰C D) ক্যালোরি /⁰C
2. SI পদ্ধতিতে J এর একক হল -
A) 4.2 x 10⁷ J/cal B) 4.2 x 10⁶ J/cal C) 4.2 J/cal D) কোনোটিই নয়
3. জলের ঘনত্ব সর্বাধিক হয় -
A) 4⁰C উষ্নতায় B) 0⁰C উষ্নতায় C) 100⁰C উষ্নতায় D) -4⁰C উষ্নতায়
4. জলের বাষ্পীভনের লীনতাপ হল -
A) 540 cal/gm B) 80 cal/gm C) 22.68 x 10⁵ cal/gm D) কোনোটিই নয়
5. বরফ গলনের সময় তার উষ্নতা -
A) বাড়ে B) কমে C) একই থাকে D) পরিবর্তিত হয়
6.শিশির জমার উপযোগী নয় -
A) মেঘমুক্ত পরিষ্কার আকাশ B) স্থির বায়ু C) মেঘলা আকাশ D) জলীয় বাষ্পের আধিক্য
7. 0⁰C উষ্নতার 10 g জলকে 100⁰C উষ্নতার বাষ্পে পরিণত করতে তাপ লাগে -
A) 6370 cal B) 1000 cal C) 5370 cal D) 100 cal
8. 0⁰C উষ্নতার 20 g বরফে 1000 cal তাপ দেওয়া হল বরফ গলনের পরিমাণ -
A) 10 g B) 15 g C) 12.5 g D) 20 g
9. যদি 100⁰C এর ফুটন্ত জল ও 100⁰C এর স্টিমে হাত দেওয়া যায় তবে -
A) 100⁰C এর জলে বেশি হাত পুড়বে B) দুটোতেই সমান হাত পুড়বে C) 100⁰C এর স্টিমে বেশি হাত পুড়বে D) কোনোটিই নয়
10. যদি ০⁰C এর জল ও ০⁰C এর বরফকে স্পর্শ করা যায় তাহলে নিচের কোন বিকল্পটি সঠিক ?
A) 0⁰C এর জল বেশি ঠান্ডা B) 0⁰C এর বরফ বেশি ঠান্ডা C) দুটোই সমান ঠান্ডা D) কোনোটিই নয়



কোন মন্তব্য নেই:
একটি মন্তব্য পোস্ট করুন